
La Anmat inhibió a un reconocido laboratorio de Quilmes por deficiencias graves en la producción de medicamentos
LOCALES21/11/2025 Esteban Díaz Romero
Esteban Díaz Romero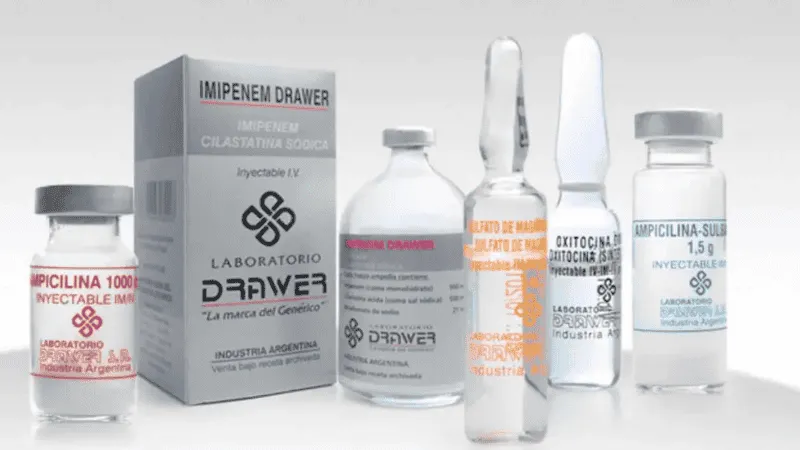
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (Anmat) decidió suspender de manera preventiva la actividad productiva de la empresa Drawer S.A., luego de detectar fallas graves durante una inspección reciente. El laboratorio, ubicado en Quilmes y dedicado desde 1985 a fabricar y comercializar medicamentos hospitalarios, fue notificado por el organismo tras comprobarse deficiencias catalogadas como críticas y mayores.
Según el documento, de acuerdo a lo que consignó Noticias Argentinas, estas irregularidades “podrían comprometer la calidad, seguridad y eficacia de los productos elaborados en el establecimiento”.
Después del relevamiento, las autoridades emitieron una carta de advertencia que establece la suspensión temporal de la elaboración y venta de productos.
Allí se detalla que “en la inspección entre los días 11 al 18 de noviembre de 2025, la comisión actuante de inspectores del Departamento de Inspectorado de la Dirección de Fiscalización y Gestión de Riesgo del Instituto Nacional de Medicamentos ha detectado y documentado en el reporte de inspección no conformidades con respecto a la normativa nacional vigente de Buenas Prácticas (BP), para Elaboradores/exportadores de Medicamentos”.
Entre los problemas detectados, se destacó la falta de información sobre la “integridad de datos, ausencia de trazabilidad de registros entre otros, deficiencias en producción; áreas limpias con clasificación deficiente, ausencia de monitoreo adecuado; dotación de personal insuficiente; deficiente calificación y cualificación de personal; el laboratorio de control de calidad exhibe deficiencias metodológicas y documentales que afectan la confiabilidad analítica; entre otros”.
Además, el organismo dispuso la prohibición de uso, venta y distribución en todo el país, y ordenó a Drawer S.A. retirar del mercado cuatro lotes específicos:
DICLOFENAC DRAWER / DICLOFENAC SODICO (COMO DICLOFENAC EPOLAMINA), 75 mg/3 ml, solución inyectable, Certificado N° 51.815, lote 90700, vencimiento 09/2027.
VANCOMICINA DRAWER / VANCOMICINA (COMO CLORHIDRATO), 1000 mg, polvo para inyectable, Certificado N° 52.491, lote 94423 (vto. 01/2027) y lote 94446.
AMPICILINA SULBACTAM DRAWER / AMPICILINA + SULBACTAM, polvo para inyectable, Certificado N° 52.569, lote 870280 (vto. 07/2027).
El documento también detalla que se inmovilizaron 139 lotes adicionales y se prohibió su uso de forma preventiva, todos enumerados en la carta de advertencia.
Finalmente, la Anmat instó a las instituciones sanitarias a “no hacer uso de dichos lotes de productos hasta tanto se establezca la medida regulatoria y concluyan las investigaciones del caso”.


Un policía de Quilmes rescató a un hombre y a un niño de una vivienda envuelta en llamas

Un hombre fue detenido tras agredir a su pareja y atacar a un policía

Aumentaron los peajes de la Autopista Bs. As. - La Plata y a la Costa Atlántica


El Municipio de Quilmes inició una actuación de oficio contra EDESUR SA por el apagón masivo de fin de año

Nicolás Maduro comparece hoy ante la justicia federal para la lectura formal de cargos

Colombia advierte que la amenaza de Trump a Petro vulnera normas del derecho internacional


Aumentaron los peajes de la Autopista Bs. As. - La Plata y a la Costa Atlántica

El Gobierno reactiva las negociaciones con los gobernadores por la reforma laboral

Un hombre fue detenido tras agredir a su pareja y atacar a un policía

Un policía de Quilmes rescató a un hombre y a un niño de una vivienda envuelta en llamas

El Municipio realizó un nuevo operativo integral de limpieza en Ezpeleta Oeste


